El primer caso de resistencia de gusanos nemátodos gastrointestinales a los antihelmínticos fue reportado ya en 1957: se trataba de un caso de resistencia de Haemonchus contortus a la fenotiazina en los EE.UU.

Hoy en día, la resistencia de los helmintos parásitos del ganado a los antiparasitarios antihelmínticos está muy extendida en los principales países tradicionalmente productores de lanares como (p.ej. Australia, Inglaterra, Nueva Zelanda; en América Latina p.ej. en Argentina, Brasil, México, Paraguay e Uruguay). Es es un problema muy grave en ovinos y caprinos, y grave en bovinos y equinos.
La resistencia de los gusanos gastrointestinales a los antiparasitarios internos afecta sobre todo a los antihelmínticos de amplio espectro más empleados en el ganado, es decir a los benzimidazoles (albendazol, fenbendazol, oxfendazol, etc.), al levamisol y a los endectocidas (ivermectina, doramectina, moxidectina, etc.).
En porcinos, mascotas y aves el problema es mucho menor por ahora.
Los mecanismos de resistencia a estos antihelmínticos son de diverso tipo y no se han elucidado en detalle en todos los casos. Para consultar los artículos en este sitio sobre dichos mecanismos de resistencia tanto a los parásitos internos como a los externos pulse aquí.
Especies de nematodos gastrointestinales resistentes a los antihelmínticos
En ovinos, y desde el punto de vista de las especies de nematodos gastrointestinales más resistentes, destacan los del género Haemonchus para los que se han confirmado casos de resistencia a los benzimidazoles (albendazol, oxfendazol, fenbendazol, etc.), al levamisol, a los endectocidas (ivermectina, moxidectina, doramectina, etc.), a las salicilanilidas (p.ej. closantel, rafoxanida), a los organofosforados, y al tiofanato.
Hay asimismo ya numerosos casos de resistencia múltiple de Haemonchus a los benzimidazoles y al levamisol en muchas propiedades de numerosos países. La resistencia de Haemonchus a los antiparasitarios antihelmínticos es especialmente problemática y preocupante, porque se trata precisamente del gusano gastrointestinal más dañino en ovinos.
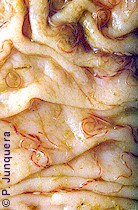
Tras Haemonchus siguen los helmintos de los géneros Ostertagia (=Teladorsagia) y Trichostrongylus, para los que hay casos confirmados de resistencia a los benzimidazoles, al levamisol y a los endectocidas. Para el género Nematodirus hay reportes de resistencia sobre todo a los benzimidazoles.
En bovinos, si bien la prevalencia y extensión de la resistencia a los antihelmínticos es notablemente menor que en ovinos, desde el punto de vista de las especies de nematodos gastrointestinales afectadas, destacan las del género Cooperia con casos de resistencia confirmada a los benzimidazoles al levamisol y a los endectocidas, así como las de géneros Haemonchus, Oesophagostomum, Ostertagia (Teladorsagia), Trichostrongylus y Trichuris con casos confirmados de resistencia a los benzimidazoles, al levamiso o a endectocidas.
Hay también reportes de casos de resistencia de Chabertia, pero se trata hasta ahora más bien de casos aislados.
En equinos hay reportes de resistencia al pirantel (Ciatostómidos o Pequeños estrongílidos), al parecer cruzada con el levamisol. En equinos cada vez es más problemática la resistencia de los (Ciatostómidos o Pequeños estrongílidos) y de Parascaris equorum a benzimidazoles y endectocidas.
En porcinos hay casos confirmados de resistencia de Oesophagostomum dentatum a la ivermectina.
En caninos hay reportes de resistencia de Ancylostoma al pirantel, y del gusano del corazón (Dirofilaria immitis) a los endectocidas.
Prevalencia de la resistencia de nematodos gastrointestinales a los antihelmínticos
En ovinos-caprinos, como ya se ha indicado, la prevalencia y extensión de la resistencia de los nematodos gastrointestinales a los antiparasitarios antihelmínticos es muy elevada en numerosos países de larga tradición de producción lanar. Así por ejemplo, según estudios de prevalencia relativamente recientes y más o menos extensos en cada país, el porcentaje de propiedades afectadas por resistencia a los benzimidazoles de entre las estudiadas se eleva al 97% en Uruguay, al 90% en Australia y Brasil, al 83% en Paraguay, al 83% en Francia, al 64% en Escocia, al 53% en Argentina, al 50% en México y al 41% en nueva Zelanda.
Algo menor pero no menos preocupante son los datos para el levamisol: 84% de las estancias en Brasil, 82% en Uruguay, 80% en Australia, 71% en Paraguay, 50% en Francia, 35% en España, 25% en Argentina y 24% en Nueva Zelanda.
Lo mismo ocurre con la resistencia a los endectocidas (ivermectina, moxidectina, etc.): 89% en Uruguay, 70% en Australia, 50% en Argentina, 44% en México, 35% en Escocia y 25% en Nueva Zelanda.
Y con resistencia múltiple a los benzimidazoles y al levamisol 73% en Brasil, 60% en Australia y 8% en Nueva Zelanda. En 2010 se reportó en Brasil un caso de resistencia de nematodos gastrointestinales ovinos a ¡¡siete clases químicas diferentes!! (levamisol, benzimidazoles, lactonas macrocíclicas, nitroxinil, disophenol, trichlorfon y closantel).
En bovinos faltan datos de la prevalencia de la resistencia de los nematodos gastrointestinales en la mayoría de los países, pero hay casos confirmados de resistencia a los antiparasitarios de mayor uso (benzimidazoles, levamisol, endectocidas) en la mayoría de los países de larga tradición ganadera bovina (Argentina, Australia, Brasil, Nueva Zelanda, EE.UU., etc.). También hay reportes de casos de resistencia múltiple (benzimidazoles y levamisol, benzimidazoles y endectocidas) en Argentina, Nueza Zelanda y los EE.UU.
Determinación y diagnóstico de la resistencia de nematodos a los antihelmínticos
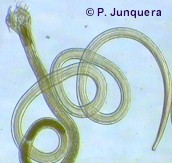
Ante la magnitud y la extensión del problema, es muy importante poder confirmar con suficiente certeza en una propiedad concreta que hay efectivamente un problema de resistencia y no se trata simplemente de uso incorrecto de un producto o de empleo de un producto inadecuado.
La primera gran dificultad para lograrlo es que los gusanos gastrointestinales no se ven a simple vista, al contrario de lo que ocurre con los parásitos externos (garrapatas, moscas, etc.). Es decir, si se administra un producto, no se ve directamente tras el tratamiento si los gusanos sobreviven o no, y si sobreviven, en qué porcentaje lo hacen.
Si efectivamente hay un problema de resistencia, el ganadero notará que el ganado, todo o parte, a pesar de haber sido tratado sigue debilitado, o con diarrea, o con anemia, u otros síntomas clínicos indicativos de problemas de gusanos gastrointestinales. Pero no sabe si se debe a gusanos o a otras razones, ni cuál es la magnitud del problema, etc.
Para confirmar un caso de resistencia no hay otra alternativa en la actualidad que hacer pruebas en las que se llevan a cabo los llamados recuentos de huevos en materia fecal de animales que han sido tratados con un antihelmíntico, y se comparan con recuentos similares de animales que no han sido tratados.
Además pues de exigir hace una prueba de campo con esos dos grupos de animales –tratados y no tratados–, hay que tomar correctamente muestras de los excrementos de los animales en el momento adecuado, y analizar dichas muestras al microscopio en laboratorios capacitados para ello, donde se determina el número de huevos de gusanos en cada muestra. En principio, para ahorrar costos y tiempo, puede prescindirse de examinar también un grupo no tratado, y contentarse con saber si en las heces del grupo tratado hay o no, más o menos gusanos supervivientes. Pero si no hay gusanos, podría ser porque los pastos estaban poco infestados, o porque casualmente esos animales observados tenían una inmunidad natural, etc., es decir, podría haber falsos negativos.
Ni que decir tiene que tales pruebas de campo deben hacerse asegurando estrictamente el uso correcto del producto. Para consultar los artículos en este sitio relativos al uso correcto de antihelmínticos pulse aquí .
El resultado de este tipo de pruebas suele consistir en afirmar que el grupo de animales no tratados (grupo control) tenia una cantidad X de huevos por gramo de materia fecal, y el grupo de animales tratados tenía una cantidad Y de huevos por gramo de materia fecal. Si Y es similar o poco inferior a X, el tratamiento no ha dado resultado y se puede decir que el producto administrado no trabaja, probablemente por desarrollo de resistencia. Si Y es notablemente menor que X (p.ej. del orden del 80-95% de X), entonces se puede decir que el producto ha trabajado bien y no hay un problema de resistencia. Algo entre medio indica que puede haber un problema de tolerancia.
Se ha investigado mucho y se sigue haciendo para desarrollar métodos más sencillos de determinación y diagnóstico rápido de la resistencia «in vitro», es decir en laboratorio, sin necesidad de hacer las ensayos de campo (basados en la eclosión de huevos, el desarrollo de larvas, la conjugación de la tubulina, análisis genómicos, etc.). Pero por ahora, estos métodos exigen instalaciones técnicas de laboratorio aún más complejas que para los recuentos fecales arriba mencionados: resumiendo, por ahora y en la mayoría de los países no hay apenas alternativas fidedignas realistas a la prueba de campo con recuento de huevos en materia fecal.
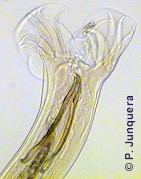
Al mismo tiempo que se confirma que hay un problema de resistencia, es necesario diagnosticar qué especie o especies de nematodos causan el problema, y qué otras especies están presentes en la propiedad. Esta es la segunda dificultad, pues por ahora esto sólo puede hacerse clasificando al microscopio los huevos hallados en las muestras fecales, algo que no es siempre sencillo de hacer y para lo que en muchos países hay pocos laboratorios lo suficientemente capacitados. Este diagnóstico es necesario para decidir seguidamente qué productos pueden considerarse para sustituir al que se ve que ya no trabaja, pues no todos los productos tiuenen el mismo espectro de acción.
Manejo de la resistencia de nematodos a los antihelmínticos en ovinos y bovinos
Por desgracia, la mayoría de los productores no podrán realizar la prueba de determinación arriba descrita con recuento de huevos en materia fecal. En estos casos puede ser útil consultar el artículo en este sitio sobre detección y diagnóstico de la resistencia (pulse aquí).
Si se llega a la conclusión de que es muy probable que haya un problema de resistencia en una propiedad, ¡¡HAY QUE CAMBIAR DE CLASE QUÍMICA DEL PRODUCTO!! A menudo habrá que hacerlo sin saber exactamente qué especie de helminto ha desarrollado resistencia, y qué otras especies están presentes en la propiedad. Por ello, si es posible, conviene cambiar a otro producto de amplio espectro.
Es ESENCIAL cambiar a un producto CON UN MECANISMO DE ACCIÓN DIFERENTE al del producto para el que ha surgido la resistencia. No basta cambiar a otra marca comercial, que puede tener el mismo principio activo u otro de la misma clase química, y que por lo tanto mostrará resistencia cruzada. Tampoco sirve cambiar de método de administración (de suspensión oral a pour-on o a inyectable). Es decir, si p.ej. se ha confirmado resistencia a un benzimidazol (albendazol, oxfendazol, fenbendazol, etc.) hay que cambiar al levamisol o a un endectocida (ivermectina, moxidectina, etc.). Según la especie de la que se trate también pueden considerarse el closantel, el morantel, la rafoxanida, u otros compuestos antihelmínticos de espectro menos amplio. El problema se agudiza si hay ya resistencia múltiple a varios antihelmínticos
En principio, si se lleva unos años (4-5) utilizando el mismo producto u otros similares de la misma clase química, conviene cambiar a otro de una clase química diferente, también si no han surgido sospechas de resistencia. Y tras 4-5 años de uso de este nuevo producto, conviene cambiar de nuevo a otro, etc. Esto es lo que se llama rotación de productos.
Ante problemas confirmados o sospechados de resistencia, suele acudirse con frecuencia a elevar la dosis del antihelmíntico. Esto NO ES RECOMENDABLE: en muchos países es ilegal, y sea legal o no, el riesgo de efectos secundarios nocivos para el ganado es real, sobre todo para animales jóvenes o debilitados. Además, los residuos serán mayores (en carne, leche, etc.), lo que obligaría a aumentar el tiempo de espera, pero ¡sin saber exactamente por cuánto tiempo! Si, por lo que sea parece imprescindible aumentar la dosis, es mejor administrar dos veces la dosis normal con un intervalo de tiempo de p.ej. 12 a 24 horas, que administrar la doble dosis de una vez. Esto es mucho más eficaz y menos arriesgado desde el punto de vista de posibles efectos secundarios para el ganado.
Los últimos nematicidas introducidos en la década de 2010 (monepantel, derquantel) permiten aún tratar los problemas de resistencia más amenazadores, si bien ya se han reportado casos de resistencia al monepantel (p.ej. en Australia, Nueva Zelanda y el Reino Unido). Pero no corre un gran riesgo de equivocarse quien prediga que, si se usa estos nuevos compuestos de modo masivo e indiscriminado como se han utilizado los hasta ahora disponibles, la extensión e indicdencia de la resistencia aumentará inexorablemente.
Urgencia de introducir el Manejo Integrado de Parásitos (MIP)
Además de un cambio de clase química una vez confirmada la resistencia en una propiedad, es tanto más urgente para el productor abandonar la actitud –si se daba– de apoyarse casi exclusivamente en el uso más o menos masivo e indiscriminado de antihelmínticos para resolver el problema de los gusanos gastrointestinales. En su lugar deben introducirse la filosofía y los métodos del Manejo Integrado de Parásitos (MIP, enlace). En el caso de los gusanos parásitos internos del ganado hay numerosas medidas preventivas que combaten el desarrollo de las poblaciones de los gusanos en los pastos y que es imperativo considerar por el productor que debe hacer frente a un problema de resistencia.
Para consultar los artículos en este sitio sobre la prevención de infecciones del ganado con gusanos parásitos pulse aquí.
En la línea del MIP, en los últimos años los expertos coinciden en recomendar reducir el número de tratamientos con antihelmínticos a lo estrictamente necesario para reducir la presión de selección, que es lo que más favorece el desarrollo de resistencia. En Australia se ha puesto en marcha el programa «Worm kill» (en español «mata gusanos») y en África del Sur el método FAMACHA. Ambos para hacer frente al problema cada vez más grave de la extensión de la resistencia de Haemonchus a los antihelmínticos en ovinos en dichos países. El objetivo es tratar sólo a los animales que realmente tienen un problema de gusanos y solo cuando el problema supera un nivel de daño determinado. Así se evita tratar animales que, aún teniendo gusanos, no sufren un daño importante.
Lo dificultoso es identificar los animales a tratar. Sólo puede hacerse mediante observación individual y regular de los posibles síntomas clínicos, y monitoreando frecuentemente la cantidad de huevos en materia fecal. El método FAMACHA se apoya en la estimación del nivel de anemia que sufre un animal debido a la infección con Haemonchus (es un gusano que chupa sangre) juzgada según el color de la mucosa interior del párpado inferior del animal (ver ilustración). En un animal sano el color es de rojo a rosa, y cuanto mayor es la anemia, tanto más pálida aparece la mucosa.
Estos métodos no son fáciles de aplicar para muchos productores y exigen un nivel considerable de capacitación y apoyo técnico. El método FAMACHA sirve sólo para Haemonchus y, por desgracia, los problemas de resistencia y de daño al ganado no sólo provienen de Haemonchus sino de muchas otras especies para las que no hay un método de diagnóstico comparablemente sencillo.
Enlaces a otros artículos sobre la resistencia en este sitio
- ¿Qué es la resistencia?
- ¿Cómo surge la resistencia?
- Tipos de resistencia
- Mecanismos de la resistencia
- Selección y refugios
- Detección y diagnóstico de resistencia
- Prevención, manejo y control de la resistencia
- Manejo integrado de parásitos
- Garrapatas y ácaros resistentes
- Moscas, pulgas y piojos resistentes
- Fasciola hepatica resistente
- RESISTENCIA A ANTIPARASITARIOS específicos